A szuperrezolúció hallatán talán a kristálytiszta, tűéles képet ígérő legújabb tévécsodák ugranak be legtöbbünknek, a mikroszkópiában azonban mást jelent ez a kifejezés. A fény hullámhossza által jelentett korlátot megkerülő technológiákról van szó, amely révén lehetséges a sejt- vagy akár molekulaszintű és a sejteken belüli élettani folyamatok megfigyelése. A pécsi Általános Orvostudományi Kar Élettani Intézetének Nano-Bio-Imaging Központjában jártunk, ahol többek között a sejtek közötti eddig ismeretlen kommunikációs formákat és azok jelentőségét kutatják a Nobel-díjat érő technológia segítségével.
Első pillantásra nem tűnik különösen izgalmasnak a pécsi orvoskar Élettani Intézetének Nano-Bio-Imaging Központja, bár a zsilipelős beléptetés jelzi, hogy nem akármilyen helyen járunk. A homályosan megvilágított teremben furcsa berendezések találhatók, mellettük pedig nagy méretű monitorokkal ellátott munkaállomások – a képernyőkön mintha színpompás absztrakt festmények képei ragyognának. Kell néhány perc ahhoz, hogy rájöjjek, elképesztő részletgazdagságban ábrázolt sejteket bámulok épp, ahogy ahhoz is, hogy feltűnjön enyhe porallergiám elmúlása.
Porallergiamentes környezet: a Nano-Bio-Imaging Központ belső tere
Mint Wilhelm Ferenctől, a központ műszaki felügyelőjétől megtudom, tünetmentességem a zsilipelős beléptetésnek és a pozitív légnyomást biztosító belső szellőztetőrendszernek köszönhető, amelyek jóvoltából a labor levegője pormentes. Az itt található berendezések ugyanis kényes jószágok, a por vagy a hőmérséklet változás hatására könnyen elállítódnak, amely akár el is lehetetlenítheti a méréseket. Ahhoz azonban, hogy megtudjuk, pontosan mik ezek a berendezések, és miért kóstálnak fejenként akár több százmillió forintot is, részt kell vennem egy rövid mikroszkópiai alapozón, amelyet a központot használó egyik kutató, Lukács András, a Biofizikai Intézet egyetemi docense tart.
Hullámhossz, az (eddigi) végső határ
„A hagyományos fénymikroszkópos technológia számára áthághatatlan határt jelent a fény hullámhossza, ez határozza meg ugyanis a felbontás maximális mértékét, azaz hogy meddig vagyunk képesek megkülönböztetni két különálló pontot. Ezt az úgynevezett diffrakciós limitet meg lehet haladni a más elven működő elektronmikroszkópok lévén, de ez a technika korlátozottan használható az élettani kutatásokban, miután vákuumban, fagyasztott mintákkal kell dolgozni, azaz esélyünk sincs az élet folyamatainak tanulmányozására. Mindez hosszú ideig meggátolta, hogy a sejtekben belüli történéseket láthassuk, és ezt a korlátot szüntette meg az úgynevezett szuperrezolúciós mikroszkópia, avagy nanoszkópia amely különböző trükkös megoldásokkal kerüli ki a fizika által jelentett határokat” – dob bele a mélyvízbe Lukács András.
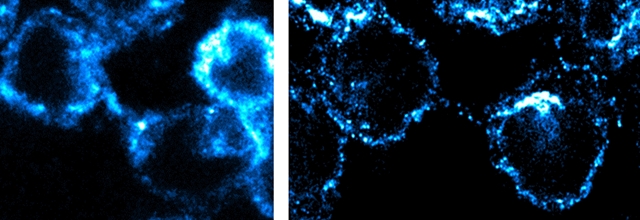
A 2014-ben kémiai Nobel-díjat érő felfedezés nyomán különböző szuperrezolúciós, azaz szuperfelbontású technológiák jelentek meg. Az egyik az úgynevezett STED mikroszkóp; itt két lézersugarat használnak az egyes pontok elkülönítéséhez, az egyik gerjeszti a molekulákat, amelyek így fluoreszcencia révén fényt bocsátanak ki, míg a másik alapállapotba juttatja vissza azokat. Az eredmény látványos: míg a monitor egyik felén a hagyományos technológiával készült „pacák” láthatóak, a másik oldalon szépen kirajzolódik a minta szerkezete – mint megtudom, épp egy sejtfelszín struktúráját szemlélem.
Szintlépés: ugyanaz a sejtstruktúra hagyományos (baloldalt) és szuperrezolúciós (jobboldalt)
Ezen a berendezésen az Élettani Intézet két kutatója, Ernszt Dávid és Godó Soma a sejtmembránt tanulmányozza. Míg egy hagyományos fénymikroszkóppal homogénnek tűnő területet láthatnánk, a szuperrezolúciónak köszönhetően egy új világ tárul elénk különféle formájú objektumokkal és struktúrákkal. Ahogy a kutatók magyarázzák, az új mikroszkópos technológiák révén azt már tudni lehet, hogy a sejtmembrán nem homogén felület, hanem egyes régiói fontos szerepet játszanak a jelátviteli folyamatokban, és most ennek kutatják a törvényszerűségeit. Mindennek nagy jelentősége lehet az agykutatásban, és egyes elméletek szerint ezeknek a régióknak a megváltozásának jelentős szerepe lehet a neurodegeneratív betegségek kialakulásában és lezajlásában.
Godó Soma kutató vizsgálatot állít be, háttérben a sejtmembrán
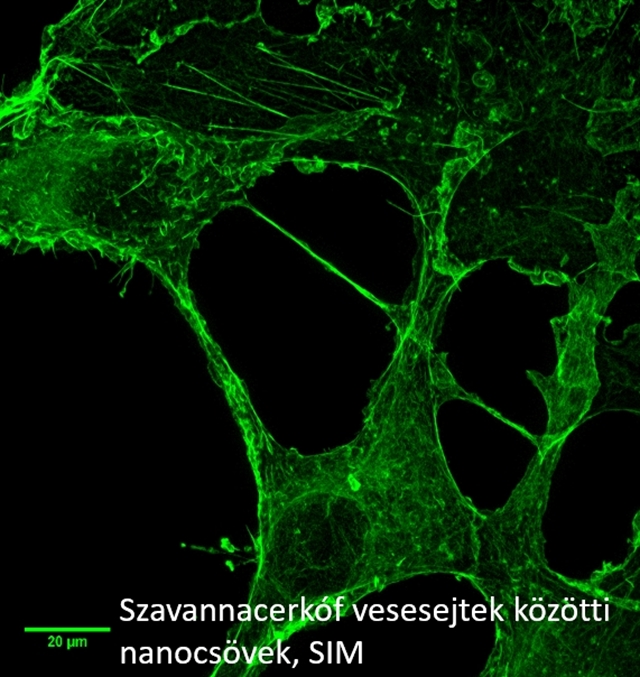
Más elven működik az N-STORM mikroszkóp, amely véletlenszerűen generált kis energiájú lézerimpulzusokkal gerjeszti a mintában található molekulákat, és aztán ezeket összerakva alkot képet, míg eggyel arrébb egy strukturált megvilágítást használó SIM mikroszkóphoz tartozó monitoron különös fonalakat, azaz a sejtek között kapcsolatot létesítő nanocsöveket lehet megszemlélni. A kutatás, illetve a felfedezés újszerűségét jól jelzi, hogy a sejtek közötti kommunikáció ismert formáit újraíró csövek még nem is kerültek be az orvosi tananyagba.
Mint kísérőim magyarázzák, minden szuperrezolúciós megoldásnak megvannak a maga előnyei és hátrányai – a STED nagyobb felbontást tesz lehetővé, mint a SIM, az utóbbiban viszont hagyományos módon preparált mintákkal is lehet dolgozni, aminek nagy gyakorlati jelentősége van; az N-STORM kiváló minőségű képet alkot, ám a véletlenszerű képalkotásnak köszönhetően meglehetősen időigényes egy kép elkészítése és így tovább. A pécsi mikroszkópközpont egyik legfőbb erőssége épp a különböző technológiák ötvözésében és ezek sokszínű felhasználásában rejlik.
Utazás a nanók földjére
A hagyományos fénymikroszkópok felbontási határa a mikrométer (a milliméter ezredrésze) körül található, míg a szuperrezolúció elvisz minket a nanométerek (a mikrométer ezredrésze) birodalmába. Ezzel a felbontással már beleláthatunk a sejtekbe és a sejtek közötti folyamatokba, és ez vezetett el a sejtek közötti nanocsövek felfedezéséhez, amelynek következményei még beláthatatlanok.
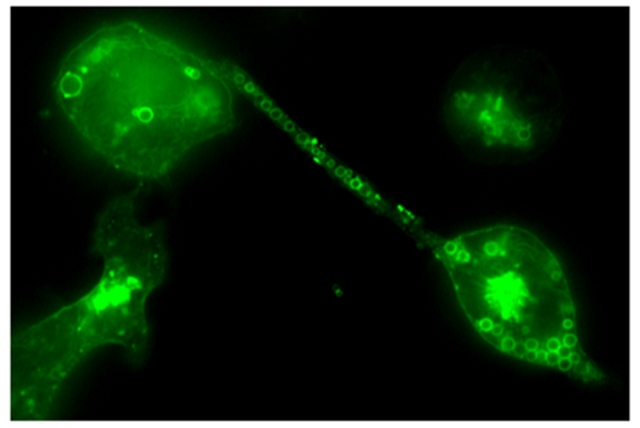
Limfóma sejtek közötti nanocsövek
A nanocsövek jó része nem éri el a 200 nanométeres szélességet sem, és épp ezért sokáig fogalma sem volt a tudósoknak a létezésükről, hiszen a hagyományos fénymikroszkópok számára ez már láthatatlan, az elektronmikroszkópok számára preparált mintákban pedig nem figyelhetők meg ezek az élő sejtek közötti kapcsolatok, magyarázza Szabó-Meleg Edina, a téma kutatója. A nanocsövek léte újraírta azt, amit a sejtek közötti folyamatokról tudunk, és a betegségek sejtszintű terjedése kapcsán is óriási jelentőségű felfedezés, mivel a kórokozók ezeken át az immunrendszert kikerülve képesek megfertőzni a sejteket – az egy helyi biotechnológiai céggel közösen zajló egyik pécsi kutatás épp a Covid–19 sejtek között történő terjedését vizsgálja egy pályázat részeként. A csövek elsődleges célja természetesen nem a vírusok számára való kiskapu biztosítása, az egyes sejtek mitokondriumot, azaz energiatermelő sejtrészecskéket adnak át például egymásnak ezeken keresztül.
Szabó-Meleg Edina a nanocsövekről tart fejtágítót
Mint ahogy a legtöbb fontos felfedezés, ez is természetesen legalább annyi kérdéshez vezet, mint amennyi választ ad. Pécsett most olyan alapvető kérdésekre keresik a választ zebrahal embriók tanulmányozásával, hogy a csövek milyen sejtek között és milyen kondíciókkal jönnek létre és milyen anyagok átadása zajlik rajtuk keresztül. Az például már kiderült, hogy a „boldogtalan”, azaz különböző anyagokkal és körülményekkel stresszelt sejtek között nagyobb mértékben alakulnak ki ilyenféle kapcsolatok, amelyek révén a sejtek egymásnak segíthetnek, emellett pedig a magzati fejlődésben is valamiféle szerepet játszhatnak.
Hogyan tedd boldoggá a sejtjeidet?
Ennek egyik potenciális felhasználása az lehet, amikor a konkrét betegségek miatt „boldogtalanná” vált sejteknek juttatnak célzottan olyan anyagot, amely az egyéb alkotórészek károsítása nélkül segít rajtuk, de az ilyen gyakorlati alkalmazások még meglehetősen messze vannak. A pécsi kutatók például a szürkehályog műtétek után tanulmányozták a nanocsövek kialakulását a műtéti traumának kitett sejteken. Itt a hagyományos, a hályog „letépésével” járó eljárás után nagy számban találtak ilyen csöveket, míg a lézeres metszést alkalmazó műtétek után nem – az külön érdekesség, hogy a hagyományos, nagyobb sejtszintű traumával járó műtét után a betegek többnyire kevesebb szövődménnyel és gyorsabban gyógyulnak meg.
Miközben pedig az új felfedezések újabb kérdésekhez vezetnek, a mikroszkóp alatt látottak ellenőrzése sem gyerekjáték. Bármilyen apró környezeti változás vagy elhibázott beállítás képalkotási hibákhoz vezethet, amiket kifejezetten nehéz úgy kiszúrni, hogy a kutatók is csak most tanulják ennek a nanovilágnak a szabályait – mint ahogy Lukács András mondja, az ellenőrzési módszerekről is doktori disszertációkat lehet írni. Az is évekbe tellett, míg a klinikusok elfogadták a sejtek közötti nanocsövek létezését, mivel hiába voltak ezek láthatóak a mintákban, az élő szervezeten belüli szövetekben nehezen megtalálhatóak.
Az Élettani Intézet munkatársai (Godó Soma, Ernszt Dávid, Buzás Péter és Wilhelm Ferenc) munka közben
Szabó-Meleg Edina tovább vezet minket a mitokondriumok színpompás(nak tűnő) világában: épp ezeknek a sejtek közötti mozgásával foglalkoznak, és ez például egy olyan kutatási irány, ami világviszonylatban is újnak mondható. A mitokondriumok idegsejtek közötti vándorlásának tanulmányozása többek között közelebb vihet minket az olyan rettegett neurodegeneratív betegségek lefolyásának megértéséhez és remélhetőleg kezeléséhez, mint az Alzheimer- és a Parkinson-kór, ugyanis egyre több bizonyíték utal arra, hogy az idegsejtek károsodása a roncsolt mitokondriumok átadása révén zajlik. A gyógyszeripar egyébként már megkezdte a nanocsövek alkalmazását, bár ez még igencsak kísérleti fázisban tart: a cél az, hogy az úgynevezett nanogyöngyökbe csomagolt hatóanyagot ezeken keresztül juttassák be a megcélzott sejtekbe.
Egy évszázadra elegendő kérdés
A kutatási terület újszerűségét jól mutatja, hogy világviszonylatban sincs túl sok erre a témára dedikált hely. Ahogy a téma pécsi szakértője fogalmaz, „a két kezemen meg tudnám számolni azokat a kutatóhelyeket, ahol a nanocsövekkel foglalkoznak”. Kevés helyen áll ehhez rendelkezésre a megfelelő eszközpark, ráadásul a kutatási eredmények ellenőrzéséhez, továbbfejlesztéséhez fontos a klinikai háttér is.
A nanovilágban tett látogatásunk végén a rengeteg új kérdés mellett egy dolog tűnik biztosnak: a szuperrezolúciós mikroszkópia révén felfedezett új élettani jelenségek és folyamatok ma még beláthatatlan lehetőségeket nyújtanak az élet alapvető folyamatainak megértéséhez és ma még gyógyíthatatlan betegségek kezeléséhez. Egyik kísérőm szavaival élve a szuperrezolúció elegendő kutatási irányt ad az elkövetkező száz évre, mi laikusok pedig addig is gyönyörködhetünk az élő sejtek absztrakt festményeket idéző pompájában.
Forrás: hvg.hu